歷經各種爭議之後,國產高端疫苗終於苦盡甘來,中央流行指揮中心今(19)日宣布,高端疫苗率先通過緊急使用授權EUA,核准專案製造,最快8月中就能開始施打。
最快8月可開始施打 審查指標均高標通過
備受關注的EUA審查流程也隨之曝光,食藥署18日找來藥學、毒理學、臨床醫學等多位專家召開會議審查EUA,高端疫苗在兩項審查指標中,達到高標,中和抗體效價是AZ疫苗的3.4倍,在血清反應比率也大約達到95.5%。
 食藥署18日找來多位專家召開會議審查EUA。圖/台視新聞 製圖
食藥署18日找來多位專家召開會議審查EUA。圖/台視新聞 製圖高端EUA過關! 審查中有1專家投反對票
21名與會專家中,扣除主席不投票外,有18人同意給予EUA,1人要求補件再議,1人不同意給EUA,但不同意的原因成謎;指揮中心研發組副組長吳秀梅解釋:「專家投票是不用寫理由的,他就只有勾。」
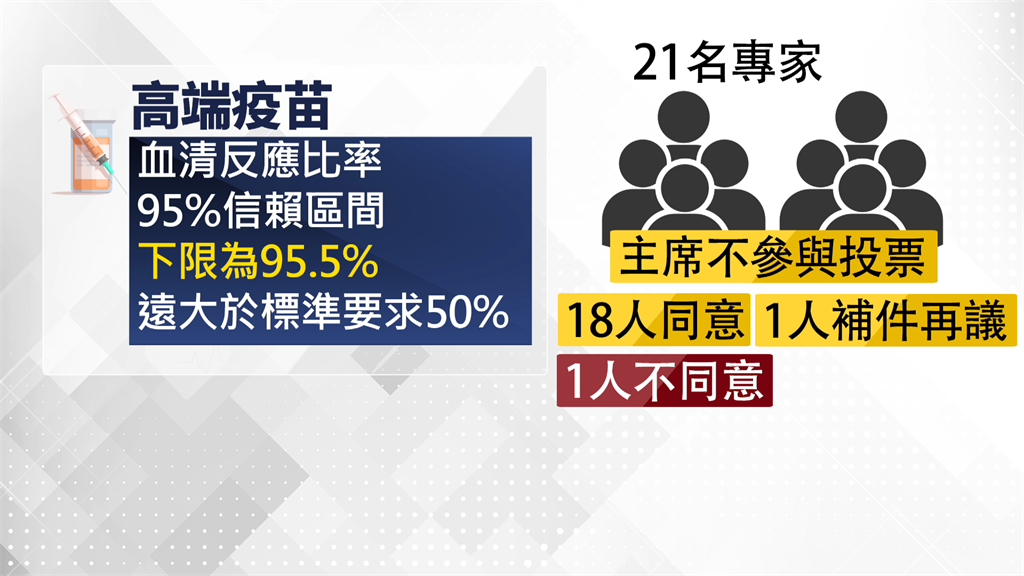 高端EUA審查投票,18人同意、1人要求補件再議、1人不同意。圖/台視新聞 製圖
高端EUA審查投票,18人同意、1人要求補件再議、1人不同意。圖/台視新聞 製圖核准提供20歲以上成人接種2劑 相隔28天
高端疫苗的開打計畫上路後,主要會提供給20歲以上成人接種,兩劑需要間隔28天,未來每個月也要提供安全監測報告,並在核准後一年內,檢送國內外執行疫苗保護效益報告;高端則強調,會再進行第三期臨床試驗還有年齡層擴充等其他驗證性試驗,以取得「常規藥證」與「國際認證」為目標。
 高端疫苗聲明。圖/台視新聞 製圖
高端疫苗聲明。圖/台視新聞 製圖審查過程未錄影 AZ比對數值未公布引質疑
只是整個EUA審查過程,沒有全程錄影,就連拿來做比較的AZ疫苗效價數字也都沒有公開,不免讓外界心生疑慮。對此指揮中心指揮官陳時中解釋,「如果全程公開,其實誰又能夠保證沒有背後的交易在,沒有公開大家講是不是有運作的空間;核准高端的MVC-COV1901,新冠肺炎疫苗的專案製造,等到我們ACIP如果通過之後,我們會看它的量能有多少,把它放到我們的施打計畫」。
高端EUA通過 黃立民:數字可以相信
對於高端疫苗通過EUA,曾在疫苗二期臨床試驗解盲時直言「別關門自嗨」的台大兒童醫院院長黃立民表示:「這數字是中研院做的,所以數字應該是可以相信,安全性我是覺得應該還可以啦,如果三期的話,大家信心就夠,沒有三期的話,每個人都不一樣。」
陳時中強調為了公平起見,會等到聯亞生技疫苗也完成審查後,自然就會公布AZ疫苗的數據資料,取信於民!
台北/魏于恬、黃明聖 責任編輯/吳東穎